Monitoraggio della formazione di di-immine con un NMR da banco

Le immine, anche dette Basi di Schiff, sono composti organici utilizzati nelle reazioni di condensazione di moltissimi materiali come leganti per produrre metalli complessi, come ad esempio il legante di Salen o quello del catalizzatore di Jacobsen. Le basi di Schiff vengono utilizzate in molti contesti industriali come ad esempio nei pigmenti a base di nichel, negli elettroliti, come nuclei bioattivi o come intermedi enzimatici.
Vista la notevole diffusione ed utilizzo è molto importante monitorare online la reazione per comprendere la formazione degli intermedi. Nello studio di questa reazione gli spettrometri NMR da banco Spinsolve, che sfrutta la tecnica della spettroscopia di risonanza magnetica nucleare, può essere un notevole aiuto.
Per valutare l’applicabilità della tecnica viene utilizzata la reazione tra fenilendiame e isobutiraldeide in acetonitrile per formare appunto una diimmina (Figura 1).
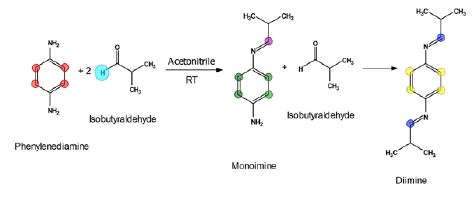
acetonitrile.
Monitoraggio online della formazione della di-immine
La reazione per formare una di–immina viene condotta in pallone, dove vengono inseriti 256mg di fenilendiammina sciolti in 22.5ml di acetonitrile anidro. Una volta disciolta si aggiungono 0.42ml di isobutiraldeide agitando la soluzione.
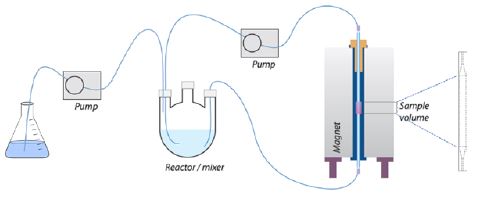
La reazione viene monitorata tramite spettro 1H NMR utilizzando lo strumento da banco Spinsolve Ultra 60 MHz dotato di kit per monitoraggio online (RMK2). Con questa configurazione è possibile eseguire il monitoraggio semi continuo (figura 2) andando a prelevare in tempi specifici la miscela dal pallone di reazione per verificare l’andamento. Durante i primi 40 minuti la miscela è stata analizzata ad intervalli di 2 minuti e successivamente ad intervalli di 10 minuti. Una volta completata la reazione sono stati confrontati gli spettri 1H 1D delle molecole di partenza con il primo e l’ultimo punto della reazione.
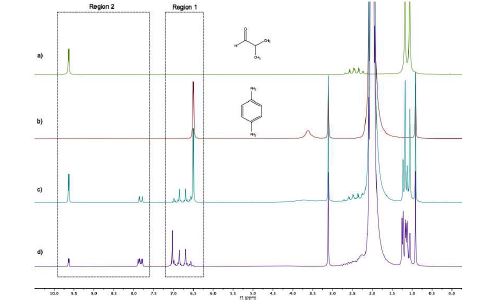
Nella figura 3 è possibile vedere i picchi caratteristici di ciascuna specie: lo spettro dell’isobutirraldeide è rappresentato nella figura3-a con picchi intorno a 9,6ppm (aldeide) a 2,3ppm (gruppo CH) e un doppietto a 1,1ppm (gruppo metilico); lo spettro della diammina è rappresentato nella figura3-b dove sono visibili i 4 singoletti dei protoni aromatici a 6,5ppm e i protoni generati dalle ammine in un grosso picco a 3,5ppm. Nella figura3-c è possibile vedere chiaramente la comparsa dei picchi di monoimina a 7,8ppm (imina), a 6,7ppm (aromatico), a 2,3ppm (CH) e a 1,1ppm (metile). Infine nella Figura3-d è visibile lo spettro finale della reazione, dove sono identificabili i segnali della diimmina che, rispetto ai segnali della monoimina, mostra dei picchi di immina e metile leggermente spostati che possono essere differenziati (figura 5). I protoni aromatici inoltre, generano un singoletto proprio come la diammina ma a 7,1ppm (figura 4).
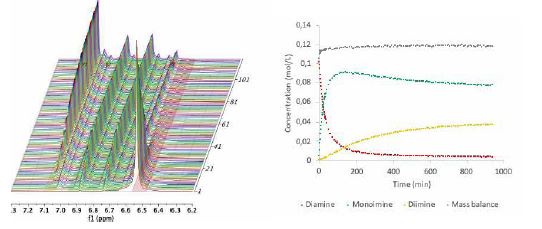
Nella figura 4 si vede un ingrandimento della regione aromatica (Regione 1 della figura 3) degli spettri eseguiti durante la reazione. Integrando i segnali corrispondenti ai diversi prodotti è possibile vedere che la concentrazione di fenilendiammina (6.54ppm) diminuisce nel tempo, mentre le concentrazioni di mono- e diimmina (6,80 e 7,06 ppm) hanno il comportamento tipico di una reazione svolta in due fasi. Dopo circa 2 ore, infatti, la concentrazione di monoimina inizia a diminuire e viene convertita in diimina.
Inoltre è possibile osservare che dopo qualche ora quasi tutte le materie prime sono scomparse, tranne la monoimina che mantiene un contenuto piuttosto elevato. Questo comportamento è tipico in reazioni in cui la costante cinetica del primo passaggio è molto più elevata di quella del secondo.
Come si può vedere dagli spettri l’evoluzione della reazione viene monitorata in modo affidabile integrando uno dei gruppi funzionali presenti nello spettro. La regione aromatica è sicuramente quella che mostra la minor sovrapposizione di segnali a differenza dei gruppi metilici che sono parzialmente sovrapposti. Infatti, dopo circa 2 ore la concentrazione di monoimina inizia a diminuire andando quasi a scomparire per convertirsi in diimina.
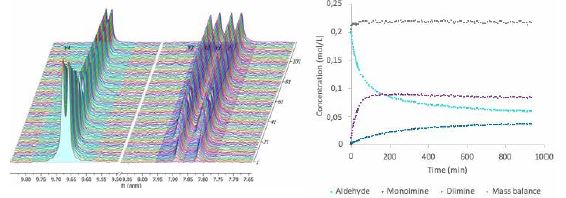
Nella figura 5 invece è visibile un ingrandimento per visualizzare meglio l’aldeide a 9,68ppm, i protoni di mono-immina e diimmina a 7,85ppm e 7,9ppm. L’aldeide è relativa ad un segnale di un composto di partenza, la mono-immina un prodotto intermedio e la diimmina un prodotto finale.
La velocità di ogni fase di reazione è molto diversa, ed è possibile osservare come la monoimina viene generata a una velocità maggiore rispetto alla diimina.
I risultati eseguiti con Spinsolve Ultra da 60MHz sono in completo accordo con quelli raccolti con un sistema da 400MHz.